病気にかかると、病院へ行き治療を施してもらいます。人によっては入院が必要となったり、薬をもらいながら長く病気と向き合ったりとさまざまです。
そんな治療法や薬を「使えるもの」「有効性のある治療方法」として確立させているのは「臨床研究」という分野です。
本稿では臨床研究とは何か、臨床研究の詳しい区分について解説します。
臨床研究とは?
厚生労働省が公表している「臨床研究に関する倫理指針」によると、「臨床研究」という言葉は以下のように定義されています。
医療における疾病の予防方法、診断方法及び治療方法の改善、疾病原因及び病態の理解並びに患者の生活の質の向上を目的として実施される次に掲げる医学系研究であって人を対象とするものをいう。
- 介入をともなう研究であって、医薬品又は医療機器を用いた予防、診断又は治療方法に関するもの
- 介入をともなう研究(①に該当するものを除く。)
- 介入を伴わず、試料等を用いた研究であって、疫学研究(明確に特定さ れた人間集団の中で出現する健康に関する様々な事象の頻度及び分布並びにそれらに影響を与える要因を明らかにする科学研究をいう。)を含まないもの(以下「観察研究」という。)
[引用元]厚生労働省:臨床研究に関する倫理指針[PDF]
https://www.mhlw.go.jp/general/seido/kousei/i-kenkyu/rinsyo/dl/shishin.pdf
つまり、臨床研究は「病気の予防・診断」「治療法の改善」「未知の病気の解明」に対して行われる医学的研究であり、結果としてそれらの研究は治療を必要とする患者、すなわち人間の命をつなぐ1つのプロセスであると考えられます。
昨今、世界を震撼させているコロナウィルスに対するワクチン・治療薬の開発、調査や病態の解明も臨床研究です。研究によって確立されたものが治療を必要とされる人たちに行き届きます。
臨床試験とは?
臨床試験は、臨床研究の枠内に含まれるものです。
その内容とは、主に患者に今後適用されるかもしれない薬剤や治療法、診断方法、予防方法に対し「安全性や有効性が確立できるのか」という視点のもと行われる試験を指します。これらをしっかり評価することで、それぞれの項目において「効果が期待できる範囲」や「禁忌」「安全性が確立できない範囲」を定めることができます。
たとえば、薬剤で「妊娠している人の服薬は禁忌」「糖尿病など自己免疫疾患をお持ちの方は服用を避けてください」といった文言を見かけたことは誰でもあるはずです。
これらは薬剤に対する臨床試験を行なった結果、判明したことで医療側からすると「必ず守って欲しいこと」です。
とくに薬剤はネットでも購入できますので「オーバードーズ(急性の有害な作用が生じるほどの量の薬を飲むこと)」のリスクや組み合わせの禁忌を考えずに飲んでしまうといった弊害のリスクが高まります。
臨床試験とは、それらを未然に防ぐための指標を作る場でもあるので、とても重要です。
では、実際にどのような臨床試験が行われているのかを見ていきましょう。
医師主導治験
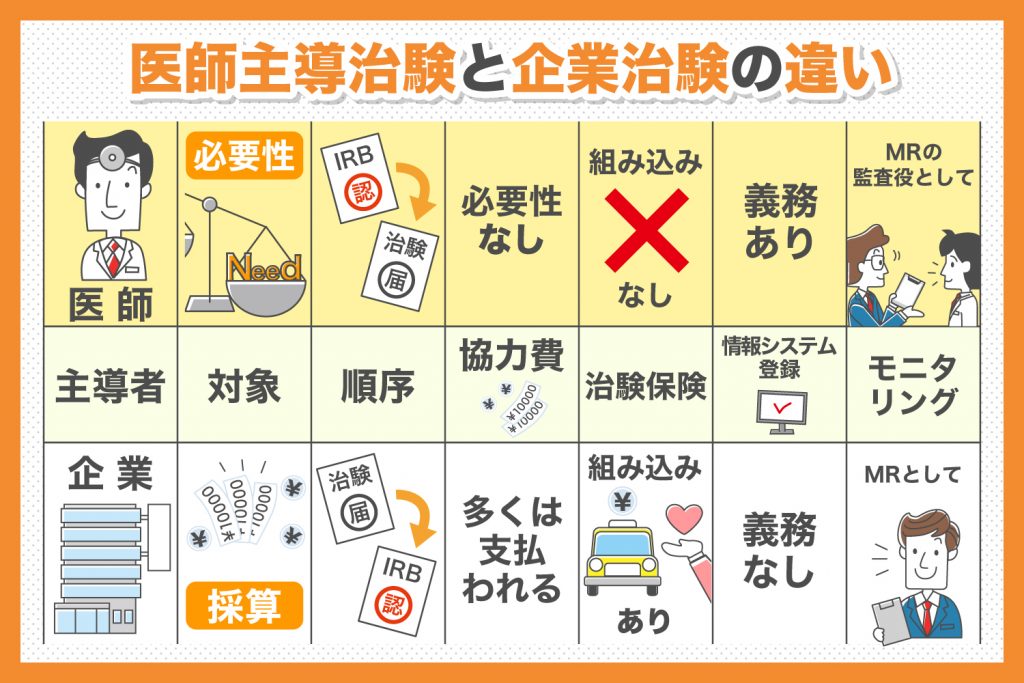
上述した企業治験と同じ「治験」に分類されるのが「医師主導治験」です。治験を行い薬剤に対して認可をもらうための方法であることは同じですが、企業治験とは以下のような点に違いが見られます。
| 項目 | 企業治験 | 医師主導治験 |
| 主導者 | 企業 | 医師 |
| 対象 | 採算に合う薬に特化している場合が多い | 医療上の必要性に基づいているものの国内では未承認の薬剤も含まれる |
| 承認・届出提出の順序 | 治験届を提出後にIRB(倫理審査委員会)の承認を得る | IRBの承認を得た後に治験届を提出する |
| 被験者への治験協力費 | 支払われることが多い | 研究費が限られるため、支払う必要性はなし |
| 治験保険 | 医療費や医療手当てが保険商品の中に組み込まれている | 医療費や医療手当てが保険商品の中に組み込まれていない |
| 情報システムへの登録 | 義務なし | 義務あり |
| 治験モニタリングを行う立ち位置 | 主にMR(医薬情報担当者)としてモニタリング | 主に医薬情報担当者監査役としてモニタリング |
なかでも大きく異なるのが、情報システムへの登録に関してです。
この情報システムへの登録は「ICMJE(International Committee of Medical Journal Editors: 医学雑誌編集者国際委員会)」の主張よって定められたもので、臨床試験すなわち医師主導治験の結果を論文として残し掲載するには必要不可欠な手続きです。
企業治験にはこのシステムへの登録義務はありませんが、医師主導治験の場合はICMJEが提示した条件を満たした登録先へ登録しないと論文が掲載されない可能性があります。
またこれらの論文は、世界各地の機関に向けて掲載されるため、英訳が必須です。医師主導治験の工程を少しでもスムーズにするためにもなるべく早い段階で登録しておいたほうがよいでしょう。
拡大治験
拡大治験とは、人間の生命に及ぼす影響が大きい疾患に対し、新しい薬を検討しなければならない場合に行なわれる臨床試験の1つです。
その治験の特殊性から「人道的見地から実施される治験」ともいわれており、独立行政法人・医薬品医療機器総合機構ではこの治験を以下のように説明しています。
生命に重大な影響がある疾患であって、既存の治療法に有効なものが存在しない疾患の治療のため、未承認薬、未承認機器及び未承認再生医療等製品(以下、「未承認薬等」という。)を臨床使用するに当たっては、当該未承認薬等の使用によるリスクと期待される治療上のベネフィットのバランスを図りつつ、当該医薬品等の開発に支障を生じないことを前提として、これらの患者からのアクセスを確保するため、治験の参加基準に満たない患者に対して人道的見地から未承認薬等を提供する制度が導入されています
[引用元] 独立行政法人 医薬品医療機器総合機構:人道的見地から実施される治験について
https://www.pmda.go.jp/review-services/trials/0016.html
ただ、この方法で治験を行なったからといって、その薬が必ずしも国内で承認されるとは限りません。あくまで未承認薬を使用する患者が得られる効果とリスクを考慮したうえで可否が判断されます。
先進医療A
先進医療とは、厚生労働省から承認を受けた高度な医療技術を用いた治療法のことを指します。
通常の医療は基本的に「公的医療保険」が用いられ、自己負担の金額を減らせますが、先進医療は保険診療外の医療行為に該当するため、公的保険を使うことはできません。
また先進医療を受けられる医療機関は限られており、厚生労働省が定める医療機関の施設基準をクリアしていないと先進医療を行うことは許されていません。
先進医療は「先進医療A」と「先進医療B」に分けられており、それぞれ技術の概要が異なります。以下は厚生労働省が定める「先進医療A」の技術概要です。
- 未承認、適応外の医薬品、医療機器の使用を伴わない医療技術
- 未承認、適応外の体外診断薬の使用をともなう医療技術等であって当該検査薬等の使用による人体への影響が極めて小さいもの
[引用元]厚生労働省:保険外併用療養費制度について[PDF]
https://www.mhlw.go.jp/file/06-Seisakujouhou-12400000-Hokenkyoku/20170925.pdf
先進医療B
厚生労働省は「先進医療B」の技術概要は以下の通りです。
- 未承認、適応外の医薬品、医療機器の使用をともなう医療技術
- 未承認、適応外の医薬品、医療機器の使用を伴わない医療技術であって、当該医療技術の安全性、有効性等に鑑み、その実施に係り、実施環境、技術の効果等について特に重点的な観察・評価を要するものと判断されるもの
[引用元]厚生労働省:保険外併用療養費制度について[PDF]
https://www.mhlw.go.jp/file/06-Seisakujouhou-12400000-Hokenkyoku/20170925.pdf
先進医療といわれている医療技術もAとBの2つに分かれます。令和2年5月1日現在、先進医療Aは22種類、先進医療Bは60種類あり、以下は、厚生労働省が公表している先進医療Aと先進医療Bの技術一覧のなかから主な先進医療技術を抜粋しまとめたものです。[注1]
<先進医療Aに区分される医療技術>
| 先進医療技術名 | 適応症 |
| 抗悪性腫瘍剤治療における薬剤耐性遺伝子検査 | 悪性脳腫瘍 |
| 腹腔鏡下膀胱尿管逆流防止術 | 膀胱尿管逆流症 |
| 陽子線治療 | 脳腫瘍を含む頭頚部腫瘍、肺・縦隔腫瘍、消化管腫瘍、肝胆膵腫瘍、泌尿器腫瘍、乳腺・婦人科腫瘍又は転移性腫瘍(根治が可能なものに限って適用) |
| 重粒子線治療 | 肺・縦隔腫瘍、消化管腫瘍、肝胆膵腫瘍、泌尿器腫瘍、乳腺・婦人科腫瘍又は転移性腫瘍(根治が可能なものに限って適用) |
| 多項目迅速ウイルスPCR法によるウイルス感染症の早期診断 | ウイルス感染症が疑われるもの |
| MRI撮影及び超音波検査融合画像に基づく前立腺針生検法 | 前立腺がんが疑われるもの(超音波検査でも病変の確認が困難な場合に限る) |
| 細胞診検体を用いた遺伝子検査 | 肺がん |
| 培養細胞によるライソゾーム病の診断 | ライソゾーム病 |
<先進医療Bに区分される医療技術>
| C型肝炎ウイルスに起因する肝硬変に対する自己骨髄細胞投与療法 | C型肝炎ウイルスによって引き起こされた肝硬変 |
| 経皮的乳がんラジオ波焼灼療法 | 長径が1.5㎝以下の早期乳がん |
| 腹腔鏡下センチネルリンパ節生検 | 早期胃がん |
| コラーゲン半月板補填材を用いた半月板修復療法 | 半月板損傷 |
| 内視鏡下手術用ロボットによる腹腔鏡下広汎子宮全摘術 | 臨床進行期分類がIA2期以上及びIIB期以下の腺がんであって、リンパ節転移及び腹腔内臓器に転移していない子宮頸がん |
| ゲムシタビン静脈内投与と重粒子線治療の併用療法 | TNM分類がT4かつ遠隔転移していないすい臓がん |
| ヒドロキシクロロキン療法 | 関節リウマチ |
| 自己軟骨細胞シートによる軟骨再生治療 | 変形性膝関節症 |
医師・研究者主導臨床試験
医師・研究者主導臨床試験とは、今まで数多くの臨床試験や治験で有効と称されてきた薬や治療法、診断方法を主な対象としています。各疾患に対してどれが最良なのか、今の薬の組み合わせよりもよい組み合わせはないのかを調べ、新たに確立させることを目的とした臨床試験のことです。
医療技術や薬は日々進化を続けており、その都度最良の方法も組み合わせも変わってきます。患者にとってよりよい医療を提供するためにも、この臨床試験は重要です。
ただ1つ心得ておかなければならないのが、未承認の薬を組み合わせとして用いる場合です。未承認である以上、組み合わせが最良ということがわかっても患者に使用することは難しいでしょう。承認を受けるために、治験が必要です。
患者申出療養
現在確立されている医療技術や治療法、治療薬では根治が難しく、未承認の薬を必要としている患者からの申し出によって行われる試験を「患者申出療法」と呼びます。
基本的に、申し出は患者本人が一定の条件を満たす医療機関(臨床研究中核病院)を通して、厚生労働省に対し行います。そこで妥当性が評価されれば実施されることがあります。
ちなみに、対象となる治療法は、科学的根拠(エビデンス)があるものでかつ一定の安全性および有効性が確認されたものに限られています。
医学の進歩に欠かせない臨床研究
臨床研究は、医療に携わる者たちにとって患者を健康にすることと同じくらい重要な仕事です。
昨今のコロナウィルスに対する治療薬やワクチンも臨床研究の積み重ねによって確立させていくものであり、この段階を飛ばして治療薬を患者に投与することはできません。
そしてこの研究は、医学の進歩と同時に患者にとっても希望を見出すものとなります。医学の進歩、そして患者の健康維持のためにも臨床研究は今後も重要視されていくでしょう。
[注1] 厚生労働省:先進医療の各技術の概要https://www.mhlw.go.jp/topics/bukyoku/isei/sensiniryo/kikan03.html
ここで解決!治験に関するFAQ
- 治験とはなんですか?
- 治験とは、『医薬品の製造販売承認申請の際に提出すべき資料のうち臨床試験の試験成績に関する資料の収集を目的とする試験の実施』、つまり、「国から薬としての販売承認を受けるために行う臨床試験」のことです。
- 治験ボランティアはアルバイト/バイトなのですか?
- 法的にはアルバイト/バイトではありません。治験ボランティア参加は負担軽減費(謝礼金)の支給がありますが、時間的拘束や、交通費などの負担を軽減する目的でお支払いするもので、治験協力費ともよばれます。
- 治験って安全ですか?副作用はありませんか?
- 治験薬は事前に生体への安全性を確認し、問題ないと予想されるものだけが使用され、治験実施についても、国の基準に沿い、参加者の方の安全に配慮した綿密な治験実施計画書に基づいて慎重に進められています。
- 健康被害が生じた場合は?
- 治験薬の副作用などにより、何らかの健康被害が生じた場合には、治験薬との因果関係が否定できない場合に限り、治験依頼者(製薬メーカー)から補償を受けることができます。補償の扱いは治験により異なりますので、それぞれの治験説明の際、医師や治験コーディネーターが詳しくお話しします。
- 都合のいい日程で参加ができますか?
- 治験の日程は予め決められております。決められた期間内での選択できる場合は、その日程内で調整していただきます。